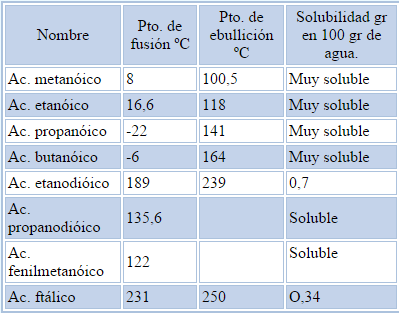
Fisicas
Solubilidad:
El grupo carboxilo -COOH confiere caracter polar a los ácidos y permite la formación de puentes de hidrógeno entre la molécula de ácido carboxílico y la molécula de agua. La presencia de dos átomos de oxigeno en el grupo carboxilo hace posible que dos moléculas se unan entre sí por puente de hidrógeno doble, formando un dímero cíclico.
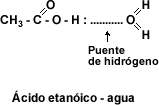
Esto hace que los primeros cuatro ácidos monocarboxílicos alifáticos sean líquidos completamente solubles en agua. La solubilidad disminuye a medida que aumenta el número de átomos de carbono. A partir del ácido láurico los ácidos caboxílicos son sólidos blandos insolubles en agua.
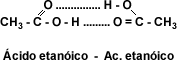
En los ácidos aromáticos monocarboxílicos, la relación carbono- carbono es de 6:1 lo que provoca que la solubilidad se vea disminuida con respecto a los ácidos monocarboxílicos alifáticos.
Punto de ebullición:
Los ácidos carboxílicos presentan puntos de ebullición elevados debido a la presencia de doble puente de hidrógeno.

Punto de fusión:
El punto de fusión varía según el número de carbonos, siendo más elevado el de los ácidos fórmico y acético, al compararlos con los ácidos propiónico, butírico y valérico de 3,4 y 5 carbonos, respectivamente. Después de 6 carbonos el punto de fusión se eleva de manera irregular.
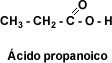
Esto se debe a que el aumento del número de átomos de carbono interfiere en la asociación entre las moléculas. Los ácidos monocarboxílicos aromáticos son sólidos cristalinos con puntos de fusión altos respecto a los ácidos alifáticos.
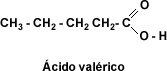
Los ácidos fórmico y acético (1,2 carbonos) son líquidos de olores irritantes. Los ácidos butíricos, valeriano y capróico (4,5 y 6 carbonos) presentan olores desagradables. Los ácidos con mayor cantidad de carbonos presentan poco olor.