Nomenclatura y Propiedades Físicas
Gran parte de las sustancias fenólicas se conocen con sus nombres comunes, por la denominación oficial de IUPAC. Por ejemplo:
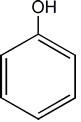
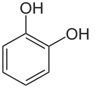
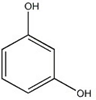
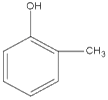
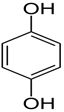
FENOL CATECOL RESORCINOL ORTO-CRESOL HIDROQUINONA
La nomenclatura se realiza en la ubicación de los diferenctes sustituyentes del anillo aromático, cuyo radical recibe el nombre de FENIL.
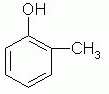
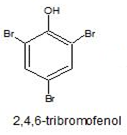
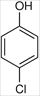
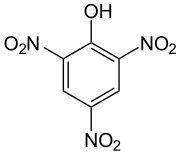
META-METIL-FENOL PARA-CLOROFENOL 2,4,6 TRINITROFENOL
Propiedades Físicas
Las moléculas de los fenoles, al igual que las de los alcoholes forman puentes de hidrógeno entre sí, por lo que presentan temperaturas de ebullición mayores que los alcanos equivalentes.
La polaridad de los fenoles se refleja igualmente en solubilidad en agua.
Los fenoles de bajo peso molecular son solubles en agua.
Si bien estos fenoles tienden a ser como ácidos o bases muy débiles, hay más ácidos que alcoholes, esto se debe a que el oxigeno en el grupo OH, está junto con el anillo aromático mas fuerte lo que el ion fenóxido es mas fijo que el alcóxido y la forma fenólica no disociada.
Por otra parte, dependiendo de su estructura, estos fenoles que se sustituyen podrían ser mas o menos ácidos que el fenol. En general decimos que, los fenoles con un sustituyente que atraiga electrones es más ácido que el fenol, puesto que estabilizan al ion fenóxido al deslocalizar su carga negativa, pero los fenoles que presentan sustituyentes donadores de los electrones son menos ácidos que el fenol, ya que desestabilizan el ion fenóxido para la carga.